legame sigma e pigreco
Il legame π pi greco è un legame chimico covalente formato per sovrapposizione laterale di due orbitali di opportuna simmetria. Il Moulin è lieto di fornire un prodotto eccezionale per celebrare il 40 anniversario della Disparition dellartista Claude François che si celebra.
 |
| Differenza Tra Obbligazioni Sigma E Pi Differbetween |
Doppietti solitariIl seguente link è il mio sito web h.
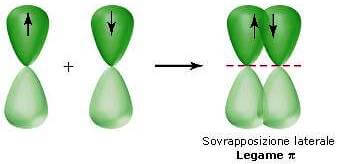
. Il legame π è meno esteso del legame σ sigma quindi il legame π è più debole del legame σ. Il legame s è più forte del legame p Un doppio legame s p è più forte di un legame singolo s ma non è due volte più forte EC-C 347 kJmol. Gli orbitali ibridi sono quasi sempre legami sigma. Legame sigma e pigreco.
La distinzione tra legami di tipo sigma e legami di tipo pi greco dipende dalla simmetria dellorbitale molecolare che descrive il legame rispetto al piano contenente i due atomi legati. Un legame sigma è un legame che si ha per sovrapposizione di orbitali lungo lasse congiungente i 2 nuclei dei 2 atomilegame frontalepertanto so. E IL DOPPIO LEGAME CC I due aroni delletene formano 2 legami tra loro. Legame sigma σ e pi greco π Le caratteristiche di un legame ovvero lunghezza e contenuto energetico dipendono dal modo in cui si sovrappongono gli orbitali atomici.
Il legame pigreco è più debole del legame sigma quindi gli alcheni reagiscono per rompere il doppio legame e formare nuovi legami sigma. Nella molecola di N 2 si realizzano un legame sigma e due legami pi greco. Tutti i legami sono di tipo sigma inoltre ci sono 2 legami pigreco che sono uno dei due legami carbonioossigeno. Il legame risultante si estende al di sopra e al di sotto il piano in cui giace il legame σ che congiunge i due stessi nuclei caratterizzato da simmetria cilindrica e presenta quindi massima densità elettronica nello spazio situato sopra e sotto il piano dei due.
Complessivamente però abbiamo che un triplo legame è più forte di un doppio legame. Già che ci sono e così ho abbastanza su cui batter ciglio per le prossime ore pongo il seguente esercizio. LEGAME PI GRECO E un legame covalente dovuto alla sovrapposizione di orbitali pparalleli Neilegami πlamassimaprobabilitàditrovareglielettronidi legameèsopra o sotto lasse internucleare. Laltro legame invece non coincide con la retta che collega i due nuclei ed è perciò un legame pi greco.
Legame semplice doppio e triplo. Più esattamente in un doppio legame uno è sigma e laltro è. La formazione del legame è spiegata sia dalla teoria del legame di valenza sia dalla teoria degli orbitali molecolari. Questo è detto DOPPIO LEGAME.
Vengono infatti a crearsi degli orbitali ibridi e quando i legami sono frontali ossia lungo lasse congiunente i nuclei dei due atomi i legami sono detti sigma mentre se i legami si trovano lateralmente alla linea congiungente sono detti pigreco. Le caratteristiche del legame π. Il legame pigreco avviene tra atomi legati da doppi o tripli legami. La sovrapposizione head-on è più profonda di quella sideways.
Il primo legame avviene lungo la congiungente si forma un legame sigma pp. Se due atomi condividono due o più coppie di elettroni la prima coppia forma un legame σ mentre le altre formano dei legami π. Quando lorbitale di un atomo si sovrappone allorbitale di un altro atomo si forma un legame covalente con la compartecipazione di una coppia di. Indicare il numero di legami sigma e pi-greco in.
Legami sigma e legami pi-greco. Il legame tra due atomi uno di fianco allaltro dove i due orbitali di ciascun atomo non si allungano lungo lasse che unisce i due atomi ma semplicemente si affiancano si chiama pigreco. Questo legame è formato dalla sovrapposizione di un orbitale p x e un orbitale p y. E il primo legame a formarsi.
Le caratteristiche del legame sigma Il legame sigma è più esteso del legame π pi greco quindi il legame σ è più forte del legame π. I legami formati dalla sovrapposizione frontale di orbitali s di orbitali p o di orbitali ibridi sono detti legami sigma o legami σ. Il legame di tipo σ sigma avviene tra due atomi che mettono in comune un elettrone ciascuno avendo tali elettroni spin opposti e si forma con la sovrapposizione di un orbitale di un atomo con un orbitale di un altro atomo. La reazione tipica degli alcheni è quindi laddizione elettrofila nella quale un reattivo povero di elettroni H Cl attacca gli elettroni del doppio legame formando un legame sigma con uno dei carboni.
I legami pi greca hanno un piano nodale 8 dove. Prendiamo lesempio di N2 vi è un legame triplo tra gli elettroni di 2px 2py e 2pz. Tali legami non sono uguali. 73 GLI ORBITALI IBRIDI SPIEGANO ANCHE LA FORMAZIONE DEI LEGAMI MULTIPLI Nei legami sigma la densità elettronica è concentrata lungo lasse che collega i nuclei dei due atomi legati.
I due ato- mi di carbonio sono tra loro col- legati da un doppio legame. Il legame π pi greco è un legame chimico covalente formato per sovrapposizione laterale di due orbitali di opportuna simmetria. In caso contrario si parla di legame pi greco e la funzione donda cambia di segno nel. Legame sigma e legame pi greco.
Un legame risulta dalla sovrapposizione assiale di due orbitali sp2 quindi è un legame sigma s. Legame s legame p Laltro legame risulta dalla sovrapposizione laterale di due orbitali p quindi è un legame. Se tale piano non è un piano nodale per lorbitale molecolare allora si parla di legame sigma. Un legame sigma risulta perciò più forte di uno pi greca perché.
Legame covalente puro o omeopolare. Un legame singolo è sempre di tipo sigma un legame doppio è costituito da un legame sigma e. Le differenze sostanziali tra un legame Ï e uno pigreca Ï sono due-modalità di sovrapposizione-energia potenziale dellorbitale molecolare. Secondo la teoria del legame di valenza la formazione del legame covalente nella molecola di idrogeno H 2 avviene per avvicinamento e sovrapposizione di due orbitali sferici semipieni contenenti cioè un solo elettrone con formazione di un nuovo orbitale molecolare.
Lanidride carbonica ha due doppi legami ciascuno composto da un legame sigma e uno pi. Come detto per la sp 2 un legame sigma è più forte di un legame pigreco. La geometria finale della molecola vede quindi i 4 atomi coinvolti formare dei legami dove agli atomi sono disposti in linea retta cioè con un angolo da 180 così da minimizzare le interazioni. Legami covalenti sigma σ e pi greco π.
I due nuclei ed è quindi un legame sigma. Teoria del legame di valenza. Non è un caso che perché si formi un legame pi greca due atomi debbano avvicinarsi molto e ancor di più nel caso della formazione di legami delta 7.
.jpg) |
| Appunti Di Chimica E Biologia Legami Sigma E Legami Pigreco |
 |
| I Legami P Pi Greco Andrea Minini |
 |
| Legame Sigma E Pigreco Celebz Talkies |
 |
| Legame S Wikipedia |
 |
| Teoria Del Legame Di Valenza |
Posting Komentar untuk "legame sigma e pigreco"